 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
NH3的分解反应为2NH3(g)N2(g)+3H2(g),在673K和100kPa总压下NH3(g)的解离度为98%,求该温度下反应的。
NH3的分解反应为2NH3(g) N2(g)+3H2(g),在673K和100kPa总压下NH3(g)的解离度为98%,求该温度下反应的
N2(g)+3H2(g),在673K和100kPa总压下NH3(g)的解离度为98%,求该温度下反应的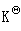 。
。
 答案
答案
KΘ=989
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
NH3的分解反应为2NH3(g) N2(g)+3H2(g),在673K和100kPa总压下NH3(g)的解离度为98%,求该温度下反应的
N2(g)+3H2(g),在673K和100kPa总压下NH3(g)的解离度为98%,求该温度下反应的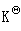 。
。
 答案
答案
KΘ=989
 更多“NH3的分解反应为2NH3(g)N2(g)+3H2(g),在673K和100kPa总压下NH3(g)的解离度为98%,求该温度下反应的。”相关的问题
更多“NH3的分解反应为2NH3(g)N2(g)+3H2(g),在673K和100kPa总压下NH3(g)的解离度为98%,求该温度下反应的。”相关的问题
第1题
A.ΔrHθm=2ΔfHθm,NH3
B.ΔrHθm=ΔfHθm,NH3
C.ΔrHθm=-2ΔfHθm,NH3
D.ArHθm=-ΔfHθm,NH3
第2题
1100K时NH3(g)在w上的分解数据如下:

试证明此反应为零级反应,求平均k.
第3题
A.升高温度使吉布斯自由能变和和标准吉布斯自由能变均增大
B.升高温度可以使平衡向右移动
C.升高温度可以使平衡常数增大
D.正反应自发时,随着反应进行,N2和H2分压逐渐减小,NH3分压逐渐增大,所以平衡常数Kp逐渐增大
第4题
从NH3(g)制备HNO3的一种工业方法是将NH3(g)与空气的混合物通过高温下的金属Pt催化剂,主要反应为4NH3(g)+5O2(g)===4NO(g)+6H2O(g)。计算1073K时的标准平衡常数。设反应的NH3(g)不随温度而改变,所需热力学数据从附录查阅。
第5题
第6题
化学反应N2(g)+3H2(g)=2NH3(g),其定压反应热Qp和定容反应热Qv的相对大小是()。
A.Qp<Qv
B.Qp>Qv
C.Qp=Qv
D.无法确定
第7题
反应N2(g)+3H2(g)=2NH3(g)(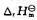 >0)达到平衡后采取下列哪种方法能使平衡向有移动。()
>0)达到平衡后采取下列哪种方法能使平衡向有移动。()
A.加入催化剂
B.降低温度
C.增加H2的压力
D.降低系统的总压
第8题
已知反应N2(g)+3H2(g)=2NH3(g)的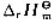 (298.15K)=-92.22kJ·mol-1若升高温度,
(298.15K)=-92.22kJ·mol-1若升高温度,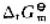 将(),
将(),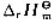 将(),
将(),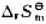 将()、
将()、 将();若减小反应系统体积,平衡将()移动;若加入氨气以增加总压力,平衡将()移动;若加入氢气以增加总压力,平衡将()移动;若加入氯化氧气体、平衡将()移动。
将();若减小反应系统体积,平衡将()移动;若加入氨气以增加总压力,平衡将()移动;若加入氢气以增加总压力,平衡将()移动;若加入氯化氧气体、平衡将()移动。
第10题
已知 CO2(g) NH3(g) H2O(g) CO(NH2)2(s)


通过计算说明,反应CO2(g)+2NH3(g)===H2O(g)+CO(NH2)2(s)
(1)在298K时,反应能否正向自发进行?
(2)在1000K时,反应能否正向自发进行?