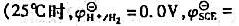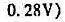题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
298K时,测得下列电池的电动势为E=0.5189V,计算该氧电极的电极溶液的pH和弱酸HA的解离常数。已知
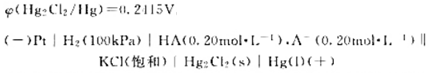
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
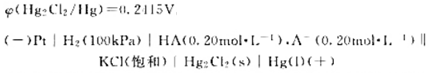
 答案
答案
 更多“298K时,测得下列电池的电动势为E=0.5189V,计算该氧电极的电极溶液的pH和弱酸HA的解离常数。已知”相关的问题
更多“298K时,测得下列电池的电动势为E=0.5189V,计算该氧电极的电极溶液的pH和弱酸HA的解离常数。已知”相关的问题
第1题
已知298K时下述电池的电动势为1.362V,
(Pt)H2(pθ)|H2SO4(aq)|Au2O3=Au(s)
又知H2O(g)的ΔrGmθ=-228.6kJ·mol-1,该温度下水的饱和蒸汽压为3167Pa,
求在298K时氧气的逸度为多少才能使Au2O3与Au呈平衡?
第2题
电池Ag(s)AgCl(s)]KCl(m)|Hg2Cl2(s)|HIg(I)的电池反应为
Ag(s)+1/2Hg2CI2(s)→AgCl(s)+Hg(I),已知298K时,此电池反应的焓变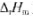 为5435/mol,各物质的规定熵数据为
为5435/mol,各物质的规定熵数据为
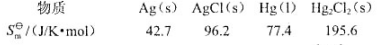 试计算该温度下电池的电动势E及电池电动势的温度系数
试计算该温度下电池的电动势E及电池电动势的温度系数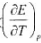
第3题
以Ag/AgC1与铜离子选择性电极组成下列电池饱和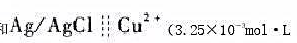
 铜离子选择性电极
铜离子选择性电极
在25℃时,测得电池的电动势为0.124V。若用未知铜活度的溶液取代上述电池中Cu2+(3.25X10-3mo1•L-1)的溶液,测得其电动势为0.086V。计算未知液中pCu(不考虑液接电位)。
第4题
自发电池: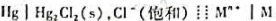 。在25℃时,测得电动势为0.100V,如将Mn+浓度稀释50倍,测得电池电动势为0.050V,此时金属离子的电荷数n是多少?
。在25℃时,测得电动势为0.100V,如将Mn+浓度稀释50倍,测得电池电动势为0.050V,此时金属离子的电荷数n是多少?
第6题
测得下列电池的电动势为0.873V(25℃)
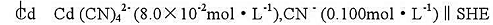
试计算Cd(CN)42-的稳定常数.
第7题
电池: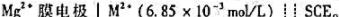 。在25℃时,测得电动势为0.387V。
。在25℃时,测得电动势为0.387V。
(1)当用未知溶液代替上述已知Mg2+溶液时。测得电池电动势为0.425V,求此溶液的pMg为多大?
(2)若溶液替代引起液接电位Ej的不稳定值为±1mV,则Mg2+浓度测定产生的相对误差有多大?波动范围为多少?
第8题
第9题
|PI的电动势为0.1705V.已知25℃时,ΔrGθm(H2SO4,水溶液)=ΔrGθm(SO42-,水溶液)=-744.53kJ·mol-1,ΔrGθm.(PbSO4,s)=-813.0kJ·mol-1.
(1)写出上述电池的电极反应和电池反应;
(2)求25°C时的 ;
;
(3)计算0.01mol.Kg-1H2SO4溶液的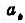 和
和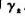 .
.
第10题
第11题
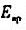 =0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。
=0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。