 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
称取一不纯有机一元弱酸试样2.3070g,其纯度为49.00%。将其溶于50.00ml水中,在25℃时,用0.2000mol
/L的NaOH溶液滴定。当中和一半弱酸时,用甘汞电极作正极,氢电极(Pt)H+/H2作负极,测其电动势为E1=0.58V,化学计量点时,测得电池电动势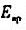 =0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。
=0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。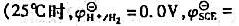
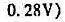
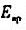 =0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。
=0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。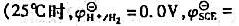
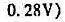
 答案
答案
查看答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
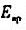 =0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。
=0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。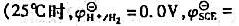
 答案
答案
 更多“称取一不纯有机一元弱酸试样2.3070g,其纯度为49.00%。将其溶于50.00ml水中,在25℃时,用0.2000mol”相关的问题
更多“称取一不纯有机一元弱酸试样2.3070g,其纯度为49.00%。将其溶于50.00ml水中,在25℃时,用0.2000mol”相关的问题
第1题
第2题
第3题
第4题
第5题
今有一PbO-PbO2混合物,现称取试样1.234g,加入20.00 mL 0.2500mol·L-1草酸溶液将PbO2还原为Pb2+,然后用氨中和,这时Pb2+以PbC2O4形式沉淀,过滤,滤液酸化后用KMnO4滴定,消耗0.04000 mol·L-1KMnO4溶液10.00mL,沉淀溶解于酸中,滴定时消耗0.04000 mol·L-1KMnO4溶液30.00mL.计算试样中PbO和PbO2的质量分数.
第6题
第7题
A.取试样一份置105℃±5℃烘箱中烘干至恒重,称取干燥集料试样的总质量,准确至0.1%
B.将试样置一洁净容器中,加入足够数量的洁净水,将集料全部淹没
C.称取每个筛上的筛余量,准确至总质量的0.1%
D.计算各筛分计筛余量及筛底存量的总和与筛分前试样的干燥总质量之比,相差不得超过筛前干燥集料质量的0.5%
E.用搪瓷盘作筛分容器,按筛孔大小排列顺序逐个将集料过筛
第8题
第9题
第10题