 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知离子半径:Ca2+99pm,Cs+182pm,S2+184pm,Br-195pm,若立方晶系CaS和CsBr晶体均服从离子晶体的结构规则,请判断这两种晶体的正、负离子的配位数,配位多面体型式,负离子的堆积方式及晶体的结构型式。
 答案
答案
查看答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“已知离子半径:Ca2+99pm,Cs+182pm,S2+184pm,Br-195pm,若立方晶系CaS和CsBr晶体均服从离子晶体的结构规则,请判断这两种晶体的正、负离子的配位数,配位多面体型式,负离…”相关的问题
更多“已知离子半径:Ca2+99pm,Cs+182pm,S2+184pm,Br-195pm,若立方晶系CaS和CsBr晶体均服从离子晶体的结构规则,请判断这两种晶体的正、负离子的配位数,配位多面体型式,负离…”相关的问题
第2题
本题通过两个箱中粒子模型的应用实例进行运算:
(1)将KCl晶体放置在金属钾蒸气中加热,K原子受辐射而电离,K→K++e-。K+扩散进入晶体,使晶体的K+离子数目多于Cl-离子数目,晶体的组成变为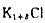 ,为了保持化合物的电中性,电子e-进入负离子的空位代替Cl-,形成
,为了保持化合物的电中性,电子e-进入负离子的空位代替Cl-,形成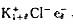 ,晶体显紫红色,这种晶体缺陷结构称色中心。已知Cl-离子半径为181pm,将电子e-看作处于立方体对角线(长为1.73×362pm)作一维势箱运动。试分别求该电子由HOMO→LUMO激发所需的能量以及由LUMO→HOMO所故出光的波长。
,晶体显紫红色,这种晶体缺陷结构称色中心。已知Cl-离子半径为181pm,将电子e-看作处于立方体对角线(长为1.73×362pm)作一维势箱运动。试分别求该电子由HOMO→LUMO激发所需的能量以及由LUMO→HOMO所故出光的波长。
(2)金属钾的摩尔体积室温时为45.36cm3mol-1,试计算它的Fermi能级(EF),分别以J和eV表示,并和实验测定值2.14eV比较。