 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知Ag+和I-离子半径分别为115和220pm,若碘化银结构完全遵循离子晶体结构规律,Ag+的配位数应为多少?实际上在常温下AgI的结构中,Ag+的配位数是多少?为什么?
 答案
答案
查看答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“已知Ag+和I-离子半径分别为115和220pm,若碘化银结构完全遵循离子晶体结构规律,Ag+的配位数应为多少?实际上在常温下AgI的结构中,Ag+的配位数是多少?为什么?”相关的问题
更多“已知Ag+和I-离子半径分别为115和220pm,若碘化银结构完全遵循离子晶体结构规律,Ag+的配位数应为多少?实际上在常温下AgI的结构中,Ag+的配位数是多少?为什么?”相关的问题
第1题
已知25℃时AgCl(s);水溶液中Ag+,CI-的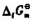 分别为-109.789kJ·mol-1,
分别为-109.789kJ·mol-1,
77.107kJ·mol-1和-131.228kJ·mol-1.求25℃下AgCl(s)在水溶液的标准溶度积Kθ及溶解度s.
第2题
已知25°C时AgCl(s).水溶液中Ag+,CI-的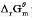 分别为-109.789kJ/mol,77.107kJ/mol和-131.22kJ/mol.求25°C下AgCl(s)在水溶液中的标准溶度积K及溶解度s。
分别为-109.789kJ/mol,77.107kJ/mol和-131.22kJ/mol.求25°C下AgCl(s)在水溶液中的标准溶度积K及溶解度s。
第5题
A.20%×15%×12%×8%
B.120%×115%×112%×108%
C.20%+15%+12%+8%
D.120%×115%×112%×108%-1
第6题
已知
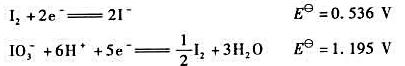
(1)试将上述两个反应的电势-pH图画在同一坐标系中;
(2)试从电势-pH图判断单质I2发生歧化反应生成I-和IO3-,的pH条件,并写出歧化反应的方程式。
第8题
第9题
Csl晶体结构类型与CsCl相同,若相邻的Cs+和I-彼此接触,已知
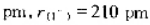 ,计算Csl晶胞边长a及晶体密度.
,计算Csl晶胞边长a及晶体密度.
第10题
A.CI-
B.I-
C.Br和I-
D.Br-