 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
C2基态为反磁性分子,试写出其电子排布.实验确定C2分子键长为124pm,比C原子共价双键半径和(2×67)pm还短,试祥明其原因.
C2基态为反磁性分子,试写出其电子排布.实验确定C2分子键长为124pm,比C原子共价双键半径和(2×67)pm还短,试祥明其原因.
 答案
答案
查看答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“C2基态为反磁性分子,试写出其电子排布.实验确定C2分子键长为124pm,比C原子共价双键半径和(2×67)pm还短,试祥明其原因.”相关的问题
更多“C2基态为反磁性分子,试写出其电子排布.实验确定C2分子键长为124pm,比C原子共价双键半径和(2×67)pm还短,试祥明其原因.”相关的问题
第2题
第4题
第6题
第7题
已知封闭的圆环中粒子的能级为
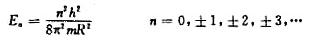
式中n为量子数,R是圆环的半径。若将此能级公式近似地用于苯分子中的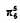 离域π键,取R=140pm,试求其电子从基态跃迁到第一激发态所吸收的光的波长。
离域π键,取R=140pm,试求其电子从基态跃迁到第一激发态所吸收的光的波长。
第8题
试写出八面体结构的配位化合物[CoCl2(NH3)4]Cl的中文名称,并回答下列各问:
(1)试画出配位单元[CoCl2(NH3)4]+的几何异构体;
(2)实验测得此配位化合物的磁矩μ=0μB。试根据配位化合物的价键理论,画出中心钴离子的d电子在轨道中的排布示意图;
(3)写出中心钴离子在成键过程中所用的杂化轨道。
第10题
试画出示意图说明下列配位单元的d轨道分裂和d电子排布情况:
(1)构型为平面正方形的配位单元[Pdl4]2-;
(2)构型为四面体的配位单元[FeCl4]-。