题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算1mol范德瓦尔斯气体在体积v1等温膨胀到v2的过程中所吸收的热量。
计算1mol范德瓦尔斯气体在体积v1等温膨胀到v2的过程中所吸收的热量。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算1mol范德瓦尔斯气体在体积v1等温膨胀到v2的过程中所吸收的热量。
 答案
答案
 更多“计算1mol范德瓦尔斯气体在体积v1等温膨胀到v2的过程中所吸收的热量。”相关的问题
更多“计算1mol范德瓦尔斯气体在体积v1等温膨胀到v2的过程中所吸收的热量。”相关的问题
第1题
证明范德瓦尔斯气体在p-v图中等温线上的极小点和极大点的轨迹方程为
pv3=a(v-2b)
第2题
1mol氢,在压强为1.0×105Pa、温度为20℃时,其体积为V0.今使它经以下两个过程达到同一状态:(1)先保持体积不变,加热使其温度升高到80℃,然后令它等温膨胀,体积变为原来的2倍;
(2)先使它等温膨胀至原体积的2倍,然后保持体积不变,加热到80℃.
试分别计算以上两种过程中吸收的热量,气体对外作的功和内能的增量;并作出p-V图.
第3题
1mol氢气在温度为300K、体积为0.025m3的状态下,经过(1)等压膨胀,(2)等温膨胀,(3)绝热膨胀.气体的体积都变为原来的两倍.试分别计算这三种过程中氢气对外作的功以及吸收的热量?
第5题
第6题
第7题
4 1mol氧气,可视为理想气体,由体积V1按照P=KV2(K为已知常数)的规律膨胀到V2,试求:
(1)气体所作的功;
(2)气体吸收的热量;
(3)该过程中气体的摩尔热容.
第9题
对于CO2气体有范德瓦耳斯常量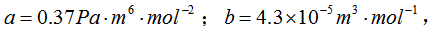 0°C时其摩尔体积为6.0x10-4m3·mol-1。试求其压强。如果将其当作理想气体处理,结果又如何?
0°C时其摩尔体积为6.0x10-4m3·mol-1。试求其压强。如果将其当作理想气体处理,结果又如何?
第10题
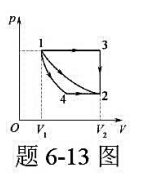
如题6-13图所示,1mol双原子分子理想气体,从初态V1=20L,T1=300K,
经历3种不同的过程到达末态V2=401,T2=300k,图中1→2为等温线,1→4为绝热线,4→2为等压线,1→3为等压线,3→2为等容线,试分别沿这3种过程计算气体的熵变。