 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用F电极和甘汞电极与溶液构成原电池,用离子计测得1.00×10-3mol·L-1NaF标液的电池
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“用F电极和甘汞电极与溶液构成原电池,用离子计测得1.00×10-3mol·L-1NaF标液的电池”相关的问题
更多“用F电极和甘汞电极与溶液构成原电池,用离子计测得1.00×10-3mol·L-1NaF标液的电池”相关的问题
第3题
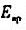 =0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。
=0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。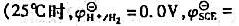
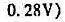
第4题
现有KNO3和NaNO2的混合样品5.000g,制备成500.0mL的溶液,移液25.00mL,用浓度为0.1200mol·L-1的Ce4+标准溶液50.00mL在强酸中氧化,过量的Ce4+用浓度为0.02500mol·L-1的Fe2+标准溶液滴定,用去Fe2+溶液28.40mL,相应的反应如下:
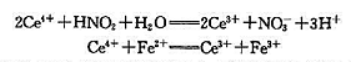
(1)若将第一个反应式作为原电池的电池反应写出该原电池的电极反应并计算该电池反应的ΔrGmθ[已知ϕθ(Ce4++/Ce3+)=1.44V,ϕθ(NO3-/NO2-)=0.934V]
(2)计算试样中NaNO2的质量分数w.[已知M(NaNO2)=69.00g.mol-1]
(3)计算第一步的标准平衡常数Kθ.
解题思路:注意原电池的写法.此题依然是考查电化与热力学、化学平衢间的计算.
第5题
A.属电位滴定法
B.以玻璃电极为指示电极,甘汞电极为参比电极
C.用标准缓冲液对仪器进行校正
D.以甘汞电极为指示电极,玻璃电极为参比电极
E.配制缓冲液与供试品的水应是新沸放冷的水
第9题