 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
称取含铝试样0.2018g,溶解后加入0.02081mol·L-1EDTA标准溶液30.00mL。调节酸度并加热使Al
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“称取含铝试样0.2018g,溶解后加入0.02081mol·L-1EDTA标准溶液30.00mL。调节酸度并加热使Al”相关的问题
更多“称取含铝试样0.2018g,溶解后加入0.02081mol·L-1EDTA标准溶液30.00mL。调节酸度并加热使Al”相关的问题
第1题
称取含铝试样1.000g,溶解后定容为250ml,移取25.00ml此试液,调节pH为9,加入8-羟基喹啉,沉淀Al3+为Al(OC9H6N)3。沉淀经过滤洗涤后,溶于HCl中,加入0.04000mol/LKBrO334.95ml(含过量的KBr),发生如下反应:
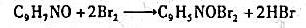
反应完成后,加入过量KI,析出I2,消耗0.1000mo/LNa2S2O3标准溶液20.00ml。计算试样中铝的质量分数。(MAl=26.98)
测定中的其他反应:
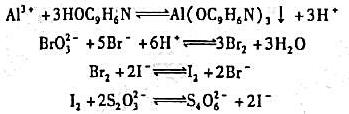
第2题
称取含NaCl试样0.5000g,溶解后加入纯AgNO3固体0.8920g,用Fe3+作指示剂,剩余的AgNO3用0.1400mol/L的KSCN溶液回滴,用去23.50ml。求试样中NaCl的质量分数。(试样中除Cl-外,不含有与Ag+生成沉淀的其他物质的离子,MAgNO3=169.9)
第3题
mol·L-1EDTA.试计算SO42-的质量分数.
第4题
第5题
重量分析法用于测定矿石中的磁铁矿(Fe3O4)的含量。称取1.5419g试样,用浓盐酸溶解后,得到Fe2+和Fe3+的混合溶液。加入硝酸将Fe2+氧化至Fe3+,稀释后用氨水将Fe3+沉淀为Fe(OH)3。将沉淀过滤,洗涤和灼烧后得0.8525gFe2O3,计算Fe2O3的质量分数?已知摩尔质量:Fe2O3为159.69g·mol-1Fe3O4为231.55g·mol-1.
第6题
第7题
于稀碱溶液中并加热(60℃)使之溶解,冷却后,加入醋酸酸化并移入250mL容量瓶中,加入0.03000mol·L-1Hg
(CIO4)2标准溶液25.00mL,稀释至刻度,放置待下述反应发生:
Hg2++2C12H11N2O3-=Hg(C12H22N2O3)2
过滤弃去沉淀,滤液用干烧杯接收.吸取25.00mL滤液,加入10mL0.01mol·L-1MgY溶液,释放出的Mg2+在pH=10时以铬黑T为指示剂,用0.0100mol·L-1EDTA滴定至终点,消耗3.60mL.计算试样中苯巴比妥钠的质量分数.
第8题
Na2S2O3溶液滴定.计算试样中KI的质量分数.
第9题
第10题
称取含惰性杂质的混合碱(Na2CO3+NaOH或Na2CO3+NaHCO3)试样0.600g,溶于水后,用0.5000mol·L-1HCl滴至酚酞褪色,用去15.00mL。然后加入甲基橙指示剂,用HCl继续滴至橙色出现, 又用去2.500mL。问试样由何种碱组成?各组分的质量分数为多少?已知M(Na2CO3)=106.00g·mol-1;M(NaOH)=40.00g·mol-1;M(NaHCO3)=84.01g·mol-1.